Haryana State Board HBSE 10th Class Science Important Questions Chapter 2 अम्ल, क्षारक एवं लवण Important Questions and Answers.
Haryana Board 10th Class Science Important Questions Chapter 2 अम्ल, क्षारक एवं लवण
अतिलघु उत्तरीय प्रश्न (Very Short Answer Type Questions)
प्रश्न 1.
अम्लों का लिटमस पर प्रभाव क्या होता है?
उत्तर-
अम्ल नीले लिटमस को लाल कर देता है।
प्रश्न 2.
लिटमस किस रंग का रंजक है?
उत्तर-
बैंगनी रंग का।
प्रश्न 3.
लिटमस किससे प्राप्त किया जाता है?
उत्तर-
थैलोफाइटा समूह के लाइकेन (Lichen) पौधे से।
प्रश्न 4.
गंधीय सूचक क्या हैं ?
उत्तर-
जिन पदार्थों की गंध अम्लीय या क्षारकीय माध्यम में बदल जाती है, उन्हें गंधीय सूचक कहते हैं।
प्रश्न 5.
गंधीय सूचकों के तीन उदाहरण लिखिए।
उत्तर-
बारीक कटी प्याज, लौंग का तेल, तनु वैनीला एसेंस।
![]()
प्रश्न 6.
हाइड्रोजन गैस किस प्रकार की ध्वनि से जलती
उत्तर-
फट-फट (Pop sound) की ध्वनि से।
प्रश्न 7.
चूने के पानी में CO2 गैस को प्रवाहित करने से क्या होता है ?
उत्तर-
चूने का पानी दूधिया हो जाता है।
प्रश्न 8.
चूने के पानी से अधिक CO2 गुजारने से चूने के पानी का दूधियापन किस कारण समाप्त हो जाता है ?
उत्तर-
जल में विलयशील Ca(HCO3)2 के कारण।
प्रश्न 9.
अधात्विक ऑक्साइड किस प्रकृति के होते हैं ?
उत्तर-
अम्लीय प्रकृति के।
प्रश्न 10.
ताँबे के बर्तन में दूध-दही क्यों नहीं रखने चाहिए?
उत्तर-
ताँबे के बर्तन में दूध-दही रखने पर वे बर्तनों के साथ अम्ल अभिक्रिया करके विषैले यौगिक (लवण) बनाते हैं।
प्रश्न 11.
अम्लों में विद्युत प्रवाह किस कारण होता है?
उत्तर-
आयनों के कारण।
![]()
प्रश्न 12.
अधिक आर्द्र गैस को किसकी सहायता से शुष्क किया जाता है ?
उत्तर-
कैल्सियम क्लोराइड की सहायता से।
प्रश्न 13.
हाइड्रोजन आयन को किस रूप में दर्शाया जाता है ?
उत्तर-
H+ (aq) या हाइड्रोनियम आयन (H3O+)।
प्रश्न 14.
अम्लों को तनु करने के लिए क्या करना चाहिए ?
उत्तर-
जल में सान्द्र अम्ल को धीरे-धीरे मिलाना चाहिए।
प्रश्न 15.
जल में अम्ल या क्षार घुलने की प्रक्रिया ऊष्माशोषी है या ऊष्माक्षेपी ?
उत्तर-
ऊष्माक्षेपी।
प्रश्न 16.
तनुकरण किसे कहते हैं ?
उत्तर-
जल में अम्ल या क्षारक मिलाने पर आयन की सान्द्रता (H3O+/OH– ) में इकाई आयतन की कमी हो जाती है जिसे तनुकरण कहते हैं।
प्रश्न 17.
अनेक सूचकों के मिश्रण को क्या कहते हैं ?
उत्तर-
सार्वत्रिक सूचक।
प्रश्न 18.
हमारा उदर कौन-सा अम्ल उत्पन्न करता है ?
उत्तर-
हाइड्रोक्लोरिक अम्ल (HCl) ।
प्रश्न 19.
हमारे शरीर में सबसे कठोर पदार्थ कौन-सा
उत्तर-
दाँतों का इनैमल (कैल्सियम फॉस्फेट)।
![]()
प्रश्न 20.
अम्लीय ऑक्साइड के नाम लिखिये जिनके द्वारा अम्लीय वर्षा होती है। (RBSE 2016)
उत्तर-
सल्फर डाइऑक्साइड (SO2) और नाइट्रोजन ऑक्साइड (NO2)।
प्रश्न 21.
अम्ल की परिभाषा लिखिए।
उत्तर-
अम्ल वे यौगिक हैं जो पानी में घुलकर हाइड्रोनियम (H3O+) को उत्पन्न करते हैं।
HCI+H2O → H3O+ + Cl–
प्रश्न 22.
क्षार की आधुनिक परिभाषा क्या है?
उत्तर-
वे यौगिक जो पानी में घुलकर OH– आयन प्रदान करते हैं, उन्हें क्षार कहते हैं, जैसे
K2O+ H2O → 2K+ + 2OH–
प्रश्न 23.
उदासीनीकरण किसे कहते हैं ?
उत्तर-
वह रासायनिक अभिक्रिया जिसमें किसी अम्ल का H+ और क्षार का OH– परस्पर मिलकर अनायनित जल अणु तैयार करे, उदासीनीकरण अभिक्रिया कहलाती है।
उदाहरण के लिए- .
HNO3 +KOH → KNO3 + H2O
प्रश्न 24.
किसी क्षार को जल में मिलाने पर क्या होता
उत्तर-
OH– जलीय आयनों की वृद्धि।
pH स्केल (pH-Scale)
प्रश्न 25.
दो संश्लेषित सूचकों के नाम लिखिये। [राज. 2015]
उत्तर-
मेथिल ऑरेंज, फीनॉल्फ्थेलिन।
प्रश्न 26.
जठर रस pH स्केल पर क्या मान दिखाता है ?
उत्तर-
लगभग 1.2.
प्रश्न 27.
सोडियम हाइड्रॉक्साइड pH स्केल पर क्या मान दिखाता है ?
उत्तर-
लगभग 14.
प्रश्न 28.
हमारा शरीर कितने pH परास के बीच कार्य करता है?
उत्तर-
हमारा शरीर 7.0 से 7.8 pH परास के बीच काम करता है।
![]()
प्रश्न 29.
किसकी pH अधिक होगी
(i) रक्त अथवा आसुत जल?
(ii) जठर रस अथवा नींबू का रस? [राज. 2015]
उत्तर-
(i) आसुत जल (pH = 7)
(ii) जठर रस (pH = 1.2)
प्रश्न 30.
मुँह में दाँतों का क्षय कब आरम्भ होता है ?
उत्तर-
pH का मान 5.5 से कम हो जाने पर दाँतों का क्षय आरम्भ हो जाता है।
प्रश्न 31.
कोई विलयन ‘X’ pH पत्र पर उसकी कोई बूंद गिराने पर नारंगी रंग देता है, जबकि कोई अन्य विलयन ‘Y’ pH पत्र पर उसकी बूंद गिराने पर हल्का नीला रंग देता है। इन दोनों विलयनों की प्रकृति क्या है? ‘X’ और ‘Y’ विलयनों के pH निर्धारित कीजिए। (CBSE 2019)
उत्तर-
‘X’ विलयन की प्रकृति अम्लीय है क्योंकि इसकी बूंदें pH पत्र पर गिराने पर वह नारंगी रंग देता है। ‘X’ विलयन का pH मान 3 से 5 के बीच हो सकता है, तथा यह हल्का अम्लीय है। Y’ विलयन की प्रकृति क्षारीय है क्योंकि इसकी बूंदें pH पत्र पर गिराने पर यह हल्का नीला रंग देता है। Y’ विलयन का pH मान 8 से 11 के बीच हो सकता है तथा यह हल्का क्षारीय है।
प्रश्न 32.
बेकिंग पॉउडर किसे कहते हैं ?(CBSE 2020)
उत्तर-
मीठा सोडा व टारटेरिक अम्ल के मिश्रण को बेकिंग पाउडर कहते हैं।
प्रश्न 33.
अग्निशमन यन्त्रों में किन रसायनों का प्रयोग किया जाता है ?
उत्तर-
हाइड्रोजन, सोडियम कार्बोनेट व सल्फ्यूरिक अम्ल का ।
प्रश्न 34.
विरंजक चूर्ण किस प्रकार के चूने से तैयार किया जाता है ? _
उत्तर-
विरंजक चूर्ण, बूझे हुए चूने [Ca(OH)2] से तैयार किया जाता है।
प्रश्न 35.
विरंजक चूर्ण को यदि वायु में खुला छोड़ दिया जाए तो क्या होगा?
उत्तर-
वायु के सम्पर्क में आने पर विरंजक चूर्ण अपघटित हो जाता है तथा क्लोरीन मुक्त होती है।
प्रश्न 36.
बिना बुझे हुए चूने का रासायनिक नाम क्या है ?
उत्तर-
कैल्सियम ऑक्साइड (CaO).
![]()
प्रश्न 37.
विरंजक चूर्ण को पानी में क्यों मिलाया जाता है ?
उत्तर–
पानी को जीवाणुरहित बनाने के लिए।
प्रश्न 38.
प्लास्टर ऑफ पेरिस बनाने के लिए किसे और कितना गर्म करना पड़ता है ?
उत्तर-
प्लास्टर ऑफ पेरिस को बनाने के लिए जिप्सम को 373 K तक गर्म किया जाता है।
प्रश्न 39.
धावन सोडा किस प्रकार का होता है ?
उत्तर-
धावन सोडा पारदर्शी क्रिस्टलीय ठोस आकार का होता है।
प्रश्न 40.
साधारण नमक किससे बनता है ?
उत्तर-
हाइड्रोक्लोरिक अम्ल (HCl) एवं सोडियम हाइड्रॉक्साइड (NaOH) की अभिक्रिया से।
लघु उत्तरीय प्रश्न (ShortAnswer Type Questions)
प्रश्न 1.
अम्लों के सामान्य गुण लिखिए।
उत्तर-
अम्लों के सामान्य गुण-
- इनका स्वाद खट्टा होता है।
- ये नीले लिटमस को लाल कर देते हैं।
- ये धातुओं के साथ क्रिया करके हाइड्रोजन गैस बनाते हैं।
- ये कार्बोनेट के साथ क्रिया करके कार्बन डाइऑक्साइड गैस उत्पन्न करते हैं।
- ये क्षारकों के साथ क्रिया करके लवण एवं पानी बनाते हैं।
प्रश्न 2.
क्षारों के सामान्य गुण लिखिए।
उत्तर-
क्षारों के सामान्य गुण-
- इनका स्वाद कड़वा होता है।
- ये लाल लिटमस को नीला कर देते हैं।
- ये अम्लों के साथ क्रिया करके लवण व पानी बनाते हैं।
- ये फीनॉल्पथेलीन के घोल को गुलाबी कर देते हैं।
प्रश्न 3.
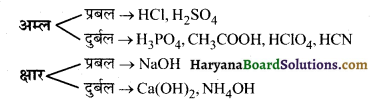
निम्नलिखित यौगिकों को दुर्बल एवं प्रबल अम्ल एवं क्षारक में वर्गीकृत कीजिए
(i) CH3COOH
(ii) NH4OH
(iii) NaOH
(iv) Ca(OH)2
(v) HCN
(vi) HClO4
(vii) H3PO4
(viii) H2SO4
(ix) HCl.
उत्तर-
प्रश्न 4.
आपको तीन परखनलियाँ A, B तथा C दी गई हैं। उनमें क्रमशः आसुत जल, एक अम्लीय विलयन तथा एक क्षारीय विलयन डाले गए हैं। आपको केवल नीले लिटमस पत्र की कतरनें दी गई हैं, इससे आप तीनों की पहचान किस प्रकार करेंगे? (CBSE 2016)
उत्तर-
- सबसे पहले तीनों लिटमस पत्र की कतरनों को प्रत्येक परखनली में डाला।
- परखनली A में रखा विलयन नीले लिटमस पत्र को लाल कर देता है जो यह दर्शाता है कि इस परखनली में रखा विलयन अम्लीय है।
- यदि शेष दो विलयनों के रंगों में किसी भी तरह का परिवर्तन नहीं होता तो इससे स्पष्ट होता है कि किसी एक विलयन में आसुत जल है तथा अन्य में क्षारीय विलयन है।
- अब परखनली A का लिटमस पत्र जो नीले रंग से लाल में परिवर्तित हो गया था को शेष दो विलयन में बारी-बारी से डाला।
- यदि परखनली B में रखा विलयन लाल लिटमस पत्र को पुनः नीले रंग में परिवर्तित कर देता है तो इससे स्पष्ट होता हे कि इस परखनली में क्षारीय विलयन है।
- परखनली C में लाल लिटमस पत्र के रंग में कोई परिवर्तन नहीं होगा अतः इस परखनली में आसुत जल है।
![]()
प्रश्न 5.
नेटल पौधे के डंकनुमा बालों के स्पर्श होने के कारण उत्पन्न पीड़ा को इसी के समीप पाये जाने वाले डॉक पौधे की पत्तियों का रस रगड़कर दूर करते हैं। इसका क्या कारण है?
उत्तर-
नेटल के पौधे में मेथेनॉइक अम्ल होता है जो शरीर में पीड़ा पहुँचाता है। चूंकि डॉक की पत्ती के रस की प्रकृति क्षारीय होती है, यह अम्ल के प्रभाव को समाप्त कर देता है और पीड़ा दूर हो जाती है।
pH- स्केल
प्रश्न 6.
लवण विलयनों के pH मान पर टिप्पणी लिखिए।
उत्तर-
प्रबल अम्ल एवं प्रबल क्षारक के लवण का pH मान 7 होता है एवं ये उदासीन होते हैं। प्रबल अम्ल और दुर्बल क्षारक के लवण के pH का मान 7 से कम होता है एवं ये अम्लीय होते हैं तथा प्रबल क्षारक एवं दुर्बल अम्ल के लवण के pH का मान 7 से अधिक होता है एवं ये क्षारकीय होते हैं।
(a) प्रबल अम्ल एवं प्रबल क्षारक के लवण NaCl, NaSO4, KCl व KNO3, आदि हैं। इन्हें जल में घोलने पर प्रबल अम्ल एवं प्रबल क्षारक बनाते हैं तथा ये पूरी तरह एक-दूसरे को उदासीन कर देते हैं।
∴ pH=7 .
(b) प्रबल अम्ल एवं दुर्बल क्षारक के लवण NH4Cl, BaCl2, ZnSO4 व CuSO4 हैं। प्रबल अम्ल दुर्बल क्षारक को प्रभावित करता है। अतः pH<7.
(c) दुर्बल अम्ल और प्रबल क्षारक के लवण Na2CO3, CH3COONa आदि हैं। प्रबल क्षारक दुर्बल अम्ल को प्रभावित करता है। अतः pH>7
(d) दुर्बल अम्ल और दुर्बल क्षारक के लवण COONH4 का विलयन लगभग उदासीन होता है।
∴ pH = 7 (लगभग)
प्रश्न 7.
उन अम्लों एवं क्षारकों की पहचान कीजिए जिनसे सोडियम हाइड्रोजन कार्बोनेट बनता है। अपने उत्तर के समर्थन में रासायनिक समीकरण लिखिए। उल्लेख कीजिए कि क्या यह यौगिक अम्लीय अथवा बारीय अथवा उदासीन है। इसका pH मान भी लिखिए। (CBSE 2019)
उत्तर-सोडियम हाइड्रोजन कार्बोनेट; दुर्बल कार्बोनिक अम्ल (H2CO3) तथा प्रबल सोडियम हाइड्रोक्साइड (NaOH) के क्षार से बनता है।
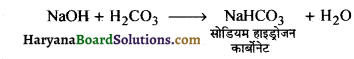
यह यौगिक एक क्षारीय यौगिक है क्योंकि यह प्रबल क्षार NaOH से बनता है। इसका pH मान 7 से थोड़ा सा अधिक है।
प्रश्न 8.
pH स्केल किसे कहते हैं? स्पष्ट करो कि मुँह का pH परिवर्तन दन्तक्षय का कारण है। (RBSE 2016)
उत्तर-
किसी विलयन में उपस्थित हाइड्रोजन आयन की सान्द्रता ज्ञात करने हेतु एक स्केल विकसित किया गया है जिसे pH स्केल कहते हैं। . मुँह के pH का मान 5.5 से कम होने पर दाँतों का इनैमल (दन्तवल्क) संक्षारित होने लगता है। दाँतों का इनमल कैल्सियम फॉस्फेट से बना होता है जोकि शरीर का सबसे कठोर पदार्थ है। मुँह में उपस्थित बैक्टीरिया, भोजन के पश्चात् मुँह में अवशिष्ट शर्करा एवं खाद्य पदार्थों का निम्नीकरण करके अम्ल उत्पन्न करते हैं।
प्रश्न 9.
अम्ल एवं क्षारक की शक्ति किस पर निर्भर करती है? प्रबल एवं दुर्बल अम्ल क्या हैं?
उत्तर-
अम्ल एवं क्षारक की शक्ति विलयन में क्रमश: (H+) आयन तथा (OH–) आयन की संख्या पर निर्भर करती है। अधिक संख्या में + आयन उत्पन्न करने वाले अम्ल प्रबल अम्ल कहलाते हैं। कम संख्या में H+ आयन उत्पन्न करने वाले अम्ल दुर्बल अम्ल कहलाते हैं।
प्रश्न 10.
धावन सोडा, जलीय विलयन में अम्लीय अथवा क्षारीय कैसे होता है ?
उत्तर-
धावन सोडा आसानी से पानी में घुल जाता है, इससे क्षारीय घोल बनता है। इसकी जाँच के लिए यदि लाल लिटमस के घोल में इसे डाला जाए तो वह नीले रंग का हो जाता है अतः धावन सोडा का घोल क्षारीय होता है।
प्रश्न 11.
खाने के सोडा के दो महत्त्वपूर्ण गुणधर्म दीजिए।
उत्तर-
खाने का सोडा सफेद रंग का क्रिस्टलीय ठोस है जो पानी के साथ क्षारीय घोल बनाता है तथा गर्म करने पर सोडियम कार्बोनेट में बदल जाता है एवं CO2, गैस उत्पन्न होती है।
![]()
प्रश्न 12.
प्लास्टर ऑफ पेरिस का रासायनिक सूत्र एवं इसकी जल के साथ रासायनिक अभिक्रिया को लिखिए। (CBSE 2020)
उत्तर-
प्लास्टर ऑफ पेरिस का रासायनिक सूत्र CaSO4.\(1 / 2\)H2O है। प्लास्टर ऑफ पेरिस एक सफेद चूर्ण है . जो जल में मिलाने पर यह पुनः जिप्सम बनकर कठोर ठोस पदार्थ प्रदान करता है।
![]()
प्रश्न 13.
उत्फुल्लन (Eflorescence) की प्रक्रिया क्या है? एक ऐसे यौगिक का नाम लिखिए जो उत्फुल्लन की क्रिया दर्शाता हो, अभिक्रिया भी लिखें।
उत्तर-
सोडियम कार्बोनेट को जब वायु में खुला छोड़ देने हैं तो सोडियम कार्बोनेट (Na2CO3, 10H2O) से जल के 9 अणु निकल जाते हैं, यह एकल हाइड्रेट (Na2CO3, H2O) के रूप में शेष रहता है। गर्म करने पर यह अपने सारे क्रिस्टलीय जल को खो देता है तथा Na2CO3, के रूप में शेष रहता है। अतः हवा में खुला रखने पर यौगिक में से जल के अणु की स्वतः मुक्त हो जाने की प्रक्रिया उत्फुल्लन (Efflorescence) कहलाती है।
![]()
प्रश्न 14.
नीचे दिए गए रासायनिक समीकरणों को पूरा और सन्तुलित कीजिये
(i) NaOH (aq) +Zn (s) →
(ii) CaCO3(s)+H20(l) +CO2(g) →
(iii) HCl(aq) + H2O(l)
अथवा
लवण जल (ब्राइन) के विद्युत अपघटन के समय एनोड पर कोई गैस ‘G’ मुक्त होती है। जब इस गैस ‘G’ को बुझे हुए चूने से प्रवाहित किया जाता है, तो कोई यौगिक ‘C’ बनता है जिसका उपयोग पीने के जल को जीवाणुओं से मुक्त करने के लिए किया जाता है।
(i) ‘G’ और ‘C’ के सूत्र लिखिए।
(ii) होने वाली अभिक्रिया का समीकरण लिखिए।
(iii). यौगिक ‘C’ का सामान्य नाम क्या है? इसका रासायनिक नाम लिखिए। (CBSE 2020)
उत्तर-
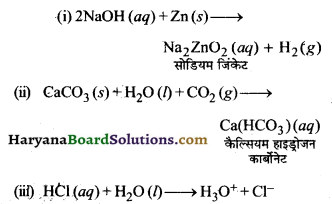
अथवा
(i) G का सूत्र = Cl2(क्लोरीन गैस) \
C का सूत्र = CaoCl2
![]()
(iii) यौगिक ‘C’ का सामान्य नाम विरंजक चूर्ण है।
यौगिक ‘C’ का रासायनिक नाम कैल्सियम ऑक्सीक्लोराइड है।
प्रश्न 15.
क्लोर-क्षार प्रक्रिया के महत्त्वपूर्ण उत्पादों की सूची बनाइए। इनमें से प्रत्येक उत्पाद का एक महत्त्वपूर्ण उपयोग लिखिए।
अथवा
सोडियम कार्बोनेट से धोने का सोडा किस प्रकार बनाया जाता है? इसका रासायनिक समीकरण लिखिए। इस लवण के प्रकार का उल्लेख कीजिए। यह जल की जिस प्रकार की कठोरता को दूर करता है, उसका नाम लिखिए। (CBSE 2020)
उत्तर-
क्लोर-क्षार प्रक्रिया के महत्त्वपूर्ण उत्पाद –
(i) सोडियम हाइड्रॉक्साइड (कास्टिक सोडा) NaOH उपयोग-इसका उपयोग साबुन तथा अपमार्जक बनाने में किया जाता है।
(ii) क्लोरीन गैस (Cl2) उपयोग-इसका उपयोग पी.वी.सी. यौगिक (एक प्रकार का प्लास्टिक) बनाने में किया जाता है।
(iii) हाइड्रोजन गैस (H2) उपयोग-इसका उपयोग राकेट ईंधन के रूप में किया जाता है।
अथवा
निर्जल सोडियम कार्बोनेटं को पानी के साथ गर्म करके क्रिस्टलन विधि द्वारा, धोने का सोडा बनाया जाता है।
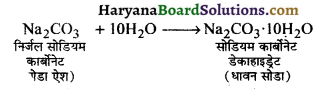
धावन सोडा एक क्षारीय लवण है। यह जल की स्थायी कठोरता दूर करता है।
प्रश्न 16.
सामान्यतः बेकरी उत्पादों में प्रयुक्त होने वाला कोईलवण ‘P’ गर्म किए जाने पर किसी अन्य लवण ‘0’ में परिवर्तित हो जाता है जिसका उपयोग जल की
कठोरता को दूर करने में किया जाता है तथा कोई गैस ‘R’ – उत्सर्जित होती है। इस गैस ‘R’ को ताजा बने चूने के पानी में से प्रवाहित करने पर वह दूधिया हो जाता है। ‘P’, ‘Q’ और ‘R’ को पहचानिए और अपने उत्तर की पुष्टि के लिए रासायनिक समीकरण दीजिए। (CBSE 2019)
उत्तर-
जब बेकिंग सोडा (NaHCO) को जल के साथ गर्म किया जाता है या मिलाया जाता है तो निम्नलिखित अभिक्रिया प्राप्त होती है।
![]()
सोडियम कार्बोनेट को जल की कठोरता दूर करने के लिए उपयोग किया जाता है। उत्सर्जित गैस कार्बन डाइऑक्साइड चूने के पानी को दूधिया कर देती है।
अतः लवण ‘P’ बेकिंग सोडा (NaHCO3) है।
लवण ‘Q’ सोडियम कार्बोनेट (Na2CO3) है जिसका प्रयोग जल की कठोरता को दूर करने के लिए किया जाता गैस ‘R’ कार्बन डाइऑक्साइड (CO2) है जो चूने के पानी को दूधिया कर देती है।
प्रश्न 17.
टूटी हड्डियों को सहारा देने के लिए डॉक्टर किसी श्वेत पाउडर का उपयोग करते हैं।
(a) इस पाउडर का नाम और रासायनिक सूत्र लिखिए।
(b) इस पाउडर को किस प्रकार बनाया जाता है।
(c) जब इस श्वेत पाउडर को पानी के साथ गूंथा जाता है, तो एक कठोर ठोस पिण्ड प्राप्त होता है। इस परिवर्तन के लिए सन्तुलित रासायनिक समीकरण लिखिए।
(d) इस श्वेत पाउडर का कोई एक और उपयोग ‘लिखिए। (CBSE 2019)
उत्तर-
(a) पाउडर का नाम-कैल्सियम सल्फेट हेमीहाइड्रेट, रासायनिक सूत्र- CaSO4\(\frac{1}{2} \) H2O
(b) जिप्सम को 100° (373 K) पर गर्म करके इस पाउडर को तैयार किया जाता है।

(d) इसका उपयोग घर के अन्दर की दीवारों तथा छत की सतह को समतल व सुंदर बनाने के लिए किया जाता है।
![]()
प्रश्न 18.
दो परखनलियों A और B जिनमें क्रमशः तनु HCIऔर NaOH विलयन भरे हैं, में नीले लिटमस का विलयन मिलाया गया है। इनमें से किस परखनली के रंग में परिवर्तन दिखाई देगा? इस रंग परिवर्तन का उल्लेख कीजिए और इसका कारण दीजिए। (CBSE 2019)
उत्तर-
परखनली A में नीले लिटमस के विलयन का रंग लाल हो जाएगा क्योंकि इस परखनली में तनु HCl अम्ल है। अम्ल नीले लिटमस को लाल रंग में परिवर्तित कर देते हैं | HCl एक प्रबल अम्ल है। इसी कारण इसे किसी विलयन में मिलाने पर H+ आयन की सांद्रता बढ़ जाती है जिससे pH मान कम हो जाता है।
प्रश्न 19.
पकौड़ों को स्वादिष्ट और खस्ता बनाने के लिए उपयोग किए जाने वाले किसी लवण का pH मान 9 है। इस लवण को पहचानिए तथा इसके निर्माण के लिए रासायनिक समीकरण लिखिए। इसके दो उपयोगों की सूची बनाइए। (CBSE 2018)
उत्तर-
पकौड़ों को स्वादिष्ट तथा खस्ता बनाने के लिए बेकिंग सोडा या सोडियम हाइड्रोजन कार्बोनेट लवण (NaHCO3) का उपयोग किया जाता है। लवण के निर्माण का रासायनिक समीकरण- .

इस लवण के दो उपयोग
- इसका उपयोग, धावन सोडा के निर्माण में किया जाता है।
- इसका उपयोग आग बुझाने के संयंत्र में किया जाता है।
प्रश्न 20.
एसीटिक अम्ल को जब एक परखनली में लिखे गये सोडियम हाइड्रोजन कार्बोनेट के पाउडर पर डालते हैं तो तेज बुलबुलों के साथ एक गैस निकलती है। इस गैस का नाम लिखिए, तथा इस गैस को पहचानने के लिए एक प्रयोग लिखिए। (CBSE 2017)
उत्तर-
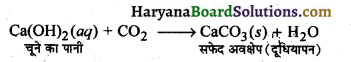
उत्पन्न होने वाली गैस CO2 है। जब CO2 गैस को चूने के पानी में से गुजारते हैं तो यह दूधिया हो जाता है।
प्रश्न 21.
उस समय आप क्या प्रेक्षण करते हैं जब आप एसीटिक अम्ल की कुछ बूंदें उस परखनली में मिलाते हैं जिसमें भरा है
(i) फिनॉल्पथैलिन
(ii) आसुत जल
(iii) सार्वत्रिक सूचक
(iv) सोडियम हाइड्रोजन कार्बोनेट चूर्ण। (CBSE 2016)
उत्तर-
(i) फिनॉल्फ्थैलिन रंगहीन रहता है, क्योंकि फिनॉल्पथैलिन अम्ल क्षारीय पदार्थों के साथ रंग में परिवर्तन • दर्शाता है।
(ii) आसुत जल में ऐसीटिक अम्ल घुल जाता है।
(iii) सार्वत्रिक सूचक नारंगी रूप में बदल जाता है।
(iv) सोडियम हाइड्रोजन कार्बोनेट चूर्ण रंगहीन हो जाता
CH3COOH + NaHCO3 → CH3COONa + H2O + CO2 ↑
दीर्घ उत्तरीय प्रश्न (Long Answer Type Questions)
प्रश्न 1.
किसी अम्ल और किसी क्षार के बीच प्रमुख अन्तर लिखिए।
उपयुक्त उदाहरणों की सहायता से पद उदासीनीकरण की व्याख्या कीजिए तथा-
(i) अम्लीय
(ii) क्षारीय और
(iii) उदासीन लवणों का बनना स्पष्ट कीजिए। (CBSE 2019)
उत्तर-
अम्ल स्वाद में खट्टे होते हैं। ये नीले लिटमस को लाल कर देते हैं। इनका pH मान 7 से कम होता है। क्षार स्वाद में कड़वे होते हैं। ये लाल लिटमस को नीला कर देते हैं। इनका pH मान 7 से अधिक होता है। जब अम्ल क्षार के साथ क्रिया करके लवण तथा जल बनाता है तो इन दोनों के बीच होने वाली इस अभिक्रिया को उदासीनीकरण क्रिया कहते हैं। सामान्यतः उदासीनीकरण अभिक्रिया को इस प्रकार लिखा जा सकता है- .
क्षार + अम्ल → लवण + जल
उदाहरण –
NaOH (aq) + HCI (aq) →NaCl (aq) + H2O (l)
(i) जब एक प्रबल अम्ल एक दुर्बल क्षार से अभिक्रिया करता है, तो बनने वाला लवण अम्लीय लवण होता है।
उदाहरण:
H2SO4+Cuo → CuSO4+ H2O
(ii) जब एक दुर्बल अम्ल एक अधिक प्रबल. क्षार से अभिक्रिया करता है तो बनने वाला लवण क्षारीय लवण होता है।
उदाहरण:
NaOH+CH3COOH → CH3COONa + H2O
(iii) जब एक प्रबल अम्ल एक प्रबल क्षार से अभिक्रिया करता है तो बनने वाला लवण उदासीन लवण होता है। उदाहरण ::… .
NaOH + HCl → NaCl+ H2O
![]()
प्रश्न 2.
निम्नलिखित लवणों के रासायनिक सूत्र लिखिए
(i) सोडियम सल्फेट ।
(ii) कैल्सियम सल्फेट
(iii) कॉपर सल्फेट
(iv) सोडियम क्लोराइड
(v) सोडियम नाइट्रेट
(vi) सोडियम कार्बोनेट
(vii) अमोनियम क्लोराइड
(viii) पोटैशियम सल्फेट।
उत्तर-
| लवण का | रासायनिक सूत्र |
| (i) सोडियमा सल्फेट | Na2SO4 |
| (ii) कैल्सियम सल्फेट | CaSO4 |
| (iii) कॉपर सल्फेट | CuSO4 |
| (iv) सोडियम क्लोराइड | Nacl |
| (v) सोडियम नाइट्रेट , | NaNO3, |
| (vi) सोडियम कार्बोनेट | NaNO3 |
| (vii) अमोनियम क्लोराइड | Na2CO3 |
| (vii) पोटैशियम सल्फेट | K2SO4 |
प्रश्न 3.
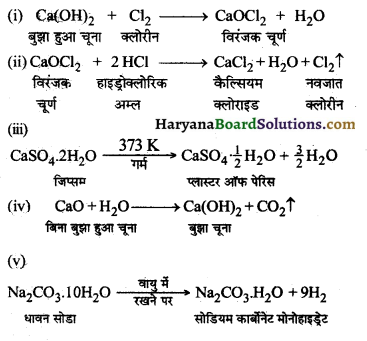
केवल रासायनिक समीकरण लिखिए –
(i) बुझे हुए चूने के साथ क्लोरीन क्रिया करती है।
(ii) विरंजक चूर्ण की तनु हाइड्रोक्लोरिक अम्ल से अभिक्रिया करायी जाती है।
(iii) जिप्सम को 373 K ताप पर गर्म किया जाता है।
(iv) चूने में पानी डाला जाता है।
(v) धावन सोडा को वायु में रखा जाता है।
उत्तर –
प्रश्न 4.
क्षारक क्या हैं? क्षारकों के गुण तथा उपयोगों का वर्णन कीजिए।
उत्तर-
जल में विलेय होने पर जो यौगिक हाइड्रॉक्साइड आयन उत्पन्न करते हैं, क्षार कहलाते हैं; जैसे-सोडियम हाइड्रॉक्साइड (NaOH), पोटैशियम हाइड्रॉक्साइड (KOH), कैल्सियम हाइड्रॉक्साइड [Ca(OH)]2 आदि। सभी क्षारकों को क्षार नहीं कहा जा सकता परन्तु सभी क्षार, क्षारक होते हैं। क्षारकों का एक उदाहरण ऐन्टैसिड है जोकि ऐलुमिनियम हाइड्रॉक्साइड तथा मैग्नीशियम हाइड्रॉक्साइड से बनता है।
मसालेदार तला भुना हुआ भोजन अधिक मात्रा में ग्रहण कर लेने पर आमाशय में अम्लता बढ़ जाती है जिसे ऐन्टैसिड के द्वारा दूर किया जाता है। क्षारकों के सामान्य गुण-क्षारकों का स्वाद तीखा एवं कड़वा होता है, स्पर्श चिकना होता है तथा प्रबल क्षार त्वचा पर संक्षारक प्रभाव डालता है। सूचकों पर इनकी क्रिया निम्न प्रकार होती है-
- लाल लिटमस को नीला कर देता है तथा नीले लिटमस पर इसका कोई प्रभाव नहीं पड़ता है।
- फिनॉल्पथेलीन तथा हल्दी के विलयन में क्षार मिलाने पर वह लाल रंग के हो जाते हैं एवं मेथिल ऑरेंज पर कोई प्रभाव नहीं पड़ता है।
- क्षारक गर्म करने पर जल उत्पन्न करते हैं तथा ऑक्साइड बनाते हैं।
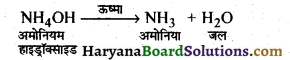
अम्लों के साथ क्षारक अभिक्रिया करके लवण तथा जल बनाते हैं। अम्ल तथा क्षारकों के बीच यह अभिक्रिया उदासीनीकरण अभिक्रिया कहलाती है।
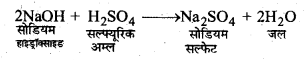
क्षारकों के जलीय विलयन हाइड्रॉक्साइड (OH–) देते हैं, प्रबल क्षारक जल में पूर्णतया विघटित हो जाते हैं, जबकि तनु क्षारक कम मात्रा में विघटित होते हैं।
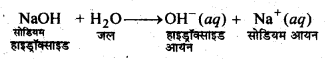
उपयोग-क्षारकों को विभिन्न प्रकार से उपयोग में लाया जाता है, जैसे-ऐलुमिनियम हाइड्रॉक्साइड का उपयोग वस्त्र उद्योग तथा ऐन्टैसिड बनाने में, अमोनियम हाइड्रॉक्साइड का उपयोग क्लीनिंग एजेण्ट तथा अमोनियम लवण बनाने में, कैल्सियम हाइड्रॉक्साइड का प्रयोग सफेदी, ब्लीचिंग पाउडर, चमड़ा उद्योग, खारे जल के शोधन आदि में तथा सोडियम हाइड्रॉक्साइड का उपयोग, साबुन, रेयान, कागज आदि उद्योगों में किया जाता है।
प्रश्न 5.
(i) हाइड्रोजन आयन [H+] की सान्द्रता का विलयन की प्रकृति पर क्या प्रभाव पड़ता है?
(ii) अम्ल को तनुकृत करते समय अम्ल को जल में मिलाया जाता है न कि जल को अम्ल में। कारण दीजिये।
(iii) संतरा और इमली में पाये जाने वाले अम्लों के नाम लिखिए।
(iv) क्लोर-क्षार प्रक्रिया किसे कहते हैं। (CBSE, RBSE 2017)
उत्तर-
(i) H+(aq) आयन की सान्द्रता का विलयन की प्रकृति पर प्रभाव पड़ता है। H+(aq) की जितनी सान्द्रता होगी, उतना ही विलयन अधिक अम्लीय होगा। जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय नहीं होता।
(ii) जल में घुलने की प्रक्रिया अत्यंत ऊष्माक्षेपी होती है। इसलिए जल में किसी सांद्र अम्ल को सावधानीपूर्वक मिलाना चाहिए। अम्ल और जल को धीरे-धीरे हिलाते रहना चाहिए। ऐसा न करने पर अम्ल में जल मिलाने पर उत्पन्न ऊष्मा के कारण मिश्रण आसफलित होकर बाहर आ सकता है। इससे स्थानीय ताप बढ़ जाता है, जिसके कारण उपयोग किया जाने वाला काँच का पात्र भी टूट सकता है।
(iii) संतरा-सिट्रिक अम्ल
इमली-टार्टरिक अम्ल
(iv) सोडियम नोराइड के जलीय विलयन (लवण जल) में विद्युत प्रवाहित करने पर यह वियोजित होकर सोडियम हाइड्रॉक्साइड उत्पन्न करता है, इसे क्लोर-क्षार प्रक्रिया कहते हैं।
2NaCl(aq) + 2H2O (l) → 2NaOH (aq) + Cl2 (g) + H2 (g)
![]()
प्रश्न 6.
हाइड्रोजन आयन की सान्द्रता ज्ञात करने में प्रयुक्त स्केल का नाम लिखिये। अम्लीय वर्षा का कारण व इसके दो कुप्रभावों को लिखिए।
उत्तर-
हाइड्रोजन आयन की सान्द्रता ज्ञात करने में pH-स्केल प्रयुक्त किया जाता है। वर्षा के जल की pH मान 5.6 से कम हो जाती है तो वह अम्लीय वर्षा (Acid Rain) कहलाती है।
अम्लीय वर्षा के कुप्रभाव-
- अम्लीय वर्षा का जल जब नदी में प्रवाहित होता है तो नदी के जल के pH का मान कम हो जाता है। ऐसी नदी में जलीय जीवधारियों की उत्तरजीविता कठिन हो जाती है।
- अम्लीय वर्षा के कारण संगमरमर से बना ताजमहल काला पड़ने लगा है क्योंकि कैल्सियम कार्बोनेट (CaCO3) वर्षा में उपस्थित अम्ल से क्रिया कर लेता है।
बहुविकल्पीय प्रश्न (Objective Type Questions)
1. विलयन में किस आयन के निर्माण के कारण पदार्थ की प्रकृति अम्लीय होती है-
(a) H+
(b) Cl –
(c) OH–
(d) SO4-2
उत्तर-
(a) H+.
2. हमारा उदर कौन-सा अम्ल उत्पन्न करता है –
(a) H2SO4
(b) HNO3
(c) HCl
(d)NaOH.
उत्तर-
(c) HCl.
3. अम्ल –
(a) का स्वाद कड़वा होता है
(b) लाल लिटमस को नीला करता है
(c) कार्बोनेट को विघटित करता है
(d) का स्पर्श फिसलने वाला होता है।
उत्तर-
(c) कार्बोनेट को विघटित्त करता है।
4. तनु अम्ल से अभिक्रिया कर कौन-सा पदार्थ CO2 उत्पन्न नहीं करेगा –
(a) संगमरमर
(b) चूना
(c) चूना पत्थर
(d) मीठा सोडा।
उत्तर-
(b) चूना।
![]()
5. हाइड्रोक्लोरिक अम्ल के जलीय विलयन में उपस्थित है –
(a) H3O+ + Cl–
(b) Cl–+OH–
(c) अनायनित HCl
(d) H3O+ + OH–
उत्तर-
(b) Cl–+OH–.
6. निम्न में से कौन-सा क्षार नहीं है-
(a)NaOH
(b) KOH
(c)NH4OH
(d) C2H5OH.
उत्तर-
(d) C2H5OH.
7. जब पानी में थोड़ी मात्रा में किसी अम्ल को मिलाते हैं तो होने वाली परिघटनाएँ हैं –
(A) तनुकरण
(B) उदासीनीकरण
(C) H3O+ आयन बनना
(D) लवण निर्मित होना
इनमें से सही कथन है-
(a)A और C
(b)B और D
(c) A और B
(d) C और D
उत्तर-
(a) A और C
8. वे पदार्थ जिनकी गंध अम्लीय या क्षारीय माध्यम में बदल जाती है, कहलाते हैं –
(a) गंधीय सूचक
(b) संश्लेषित सूचक
(c) लिटमस
(d) ये सभी सूचक।
उत्तर-
(a) गंधीय सूचक।
9. अम्ल तथा क्षारक की परस्पर क्रिया से लवण तथा पानी बनता है, यह क्रिया है-
(a) जल-अपघटन
(b) संयोजन
(c) उदासीनीकरण
(d) वैद्युत अपघटन।
उत्तर-
(c) उदासीनीकरण।
10. किसी विलयन की pH किसकी माप है
(a) हाइड्रोजन आयन सान्द्रता
(b) हाइड्रोनियम आयन सान्द्रता
(c) दोनों (a) व (b)
(d) इनमें से कोई नहीं।
उत्तर-
(c) दोनों (a) व (b).
![]()
11. रक्त का pH मान है-
(a) 0
(b) 2
(c) 4
(d) 7.4.
उत्तर-
(d) 7.4.
12. pH चार्ट के अन्तिम सिरों पर दिखने वाले दो रंग हैं
(a) लाल और नीला
(b) लाल तथा हरा
(c) हरा और लाल
(d) नारंगी तथा हरा (CBSE 2016)
उत्तर-
(a) लाल और नीला।
13. चार छात्र A,B,C,D जल,नींबू पानी तथा तनुसोडियम बाइकार्बोनेट के विलयनों का pH निकालते हैं। उन्होंने प्रेक्षणों द्वारा प्राप्त pH के नामों को अवरोही क्रम में इस प्रकार व्यवस्थित किया विलयन
A . जल, नींबू पानी, सोडियम बाइकार्बोनेट विलयन जल, सोडियम बाइकार्बोनेट विलयन, नींबू पानी – नींबू पानी, जल, सोडियम बाइकार्बोनेट
विलयन D
सोडियम बाइकार्बोनेट विलयन, जल,
नींबू पानी छात्र द्वारा सही क्रम है
(CBSE 2016)
(a) A
(b) B
(c) C
(d) D
उत्तर-
(d) D
14. आपके विद्यालय के आस-पड़ोस में प्रयोग के लिए आवश्यक कठोर जल उपलब्ध नहीं है। आपके विद्यालय में उपलब्ध लवणों के नीचे दिए गए समूहों में से वह एक समूह चुनिए जिसके प्रत्येक सदस्य को आसुत जल में घोलने पर, वह उसे कठोर जल बना देगा –
(a) सोडियम क्लोराइड, कैल्सियम क्लोराइड
(b) पौटेशियम क्लोराइड, सोडियम क्लोराइड
(c) सोडियम क्लोराइड, मैग्नीशियम क्लोराइड
(d) कैल्सियम क्लोराइड, मैग्नीशियम क्लोराइड (CBSE 2016)
उत्तर-
(d) कैल्सियम क्लोराइड, मैग्नीशियम क्लोराइड
15. कोई छात्र 25 mL धारिता की चार परखनलियों P, Q, R और S लेकर प्रत्येक परखनली में 10 mL आसुत जल भरता है। वह इन परखनलियों में चार भिन्न लवणों का एक-एक चम्मच इस प्रकार मिलाता है-P में KCl; Q में NaCl; Rमें CaCl, तथा S में MgCl, I तत्पश्चात वह प्रत्येक परखनली में साबुन के विलयन के नमूने का लगभग 2 ml डालता है। प्रत्येक परखनली के पदार्थों की भली-भाँति हिलाने पर उसे जिन परखनलियों में भरपूर झाग मिलने की सम्भावना है, वे परखनलियाँ हैं-
(a) P और Q
(b) R और S
(c) P, Q और R
(d) P, Q और S (CBSE 2016)
उत्तर-
(a) P और Q
रिक्त स्थानों की पूर्ति कीजिए (Fill In the blanks)
1. चूना-पत्थर, खड़िया और संगमरमर ………………….. के विभिन्न रूप हैं।
उत्तर-
कैल्सियम कार्बोनेट,
2. जलीय कॉपर सल्फेट का सूत्र ………………….. है।
उत्तर-
CuSO4.5H2O,
3. जिप्सम का सूत्र ………………….. है।
उत्तर-
CaSO4 . 2H2O,
4. क्षार वे पदार्थ होते हैं जो जलीय विलयन में ………………….. उत्सर्जित करते हैं।
उत्तर-
हाइड्रॉक्साइड आयन (OH–),
5. वर्षा के जल की pH मान 5.6 से कम हो जाता है तो वह ………………….. कहलाती है।
उत्तर-
अम्लीय वर्षा।
![]()
सुमेलन संबंधी प्रश्न (Matrix Type Questions)
प्रश्न 1.
निम्न को सुमेलित करें
| A | B |
| (1) जिप्सम | (a) CaoCl2 |
| (2) बेकिंग सोडा | (b) MgSO4.7H2O |
| (3) ब्लीचिंग पाउडर | (c) CasO4. \(\frac{1}{2}\)H2O |
| (4) एप्सम लवण | (d) CaO |
| (5) बिना बुझा हुआ चूना | (e) CaSO4.2H2O |
| (6) प्लास्टर ऑफ पेरिस | (f) NaHCO3, |
उत्तर-
| A | B |
| (1) जिप्सम | (e) CaSO4.2H2O |
| (2) बेकिंग सोडा | (f) NaHCO3, |
| (3) ब्लीचिंग पाउडर | (a) CaoCl2 |
| (4) एप्सम लवण | (b) MgSO4.7H2O |
| (5) बिना बुझा हुआ चूना | (c) CasO4. \(\frac{1}{2}\)H2O |
| (6) प्लास्टर ऑफ पेरिस | (d) CaO |