Haryana State Board HBSE 10th Class Science Solutions Chapter 1 रासायनिक अभिक्रियाएँ एवं समीकरण Textbook Exercise Questions and Answers.
Haryana Board 10th Class Science Solutions Chapter 1 रासायनिक अभिक्रियाएँ एवं समीकरण
HBSE 10th Class Science रासायनिक अभिक्रियाएँ एवं समीकरण Textbook Questions and Answers
प्रश्न 1.
नीचे दी गई अभिक्रिया के सम्बन्ध में कौन-सा कथन असत्य है
2 Pbo(s) +C(s) →2Pb (s)+CO2(g)
(a) सीसा अपचयित हो रहा है।
(b) कार्बन डाइऑक्साइड उपचयित हो रही है।
(c) कार्बन उपचयित हो रहा है।
(d) लैड ऑक्साइड अपचयित हो रहा है।
(i) (a) एवं (b)
(ii) (a) एवं (c)
(iii) (a), (b) एवं
(c) (iv) सभी।
उत्तर-
(i) (a) एवं (b).
कारण- उपरोक्त अभिक्रिया की विपरीत अभिक्रिया में अर्थात्
2Pb(s) + CO2(g) →2PbO(s) + C(s)
मे Pb का ऑक्सीकरण PbO में तथा CO2, का अपचयन C में हो रहा है।
प्रश्न 2.
Fe2O3+2Al → Al2O3, +2Fe
ऊपर दी गई अभिक्रिया निम्न में से किस प्रकार की है –
(a) संयोजन अभिक्रिया
(b) द्वि-विस्थापन अभिक्रिया
(c) वियोजन अभिक्रिया
(d) विस्थापन अभिक्रिया।
उत्तर-
(d) विस्थापन अभिक्रिया।
कारण- इस अभिक्रिया में एलुमीनियम (Al), Fe2O3, से Fe को विस्थापित करके AI2O3 बना रहा है अत: यह एक विस्थापन अभिक्रिया है।
![]()
प्रश्न 3.
लौह-चूर्ण पर तनु हाइड्रोक्लोरिक अम्ल डालने से निम्न में से क्या होता है?
(a) हाइड्रोजन गैस तथा आयरन क्लोराइड बनता है
(b) क्लोरीन गैस एवं आयरन हाइड्रॉक्साइड बनता है
(c) कोई अभिक्रिया नहीं होती है
(d) आयरन लवण तथा जल बनता है।
उत्तर-
(a) हाइड्रोजन गैस तथा आयरन क्लोराइड बनता है। ये अभिक्रिया निम्न प्रकार है
Fe(s) + 2HCl(dil) → FeCl2 (aq) + H2 (g)
प्रश्न 4.
सन्तुलित रासायनिक समीकरण क्या है ? रासायनिक समीकरण को सन्तुलित करना क्यों आवश्यक है ?
उत्तर-
वह रासायनिक समीकरण जिसके दोनों पक्षों में प्रत्येक तत्व के परमाणुओं की संख्या बराबर होती है, सन्तुलित रासायनिक समीकरण (Balanced Chemical Equation) कहलाता है, जैसे
निम्नलिखित अभिक्रिया में अभिकारकों तथा उत्पादों में अलग-अलग सभी तत्वों के परमाणुओं की गणना करते हैं
Zn+H2SO4 →ZnSO4 + H2
| तत्व के परमाणुओं की संख्या | अभिकारकों में | उत्पादों में |
| Zn | 1 | 1 |
| H | 2 | 2 |
| S | 1 | 1 |
| O | 4 | 4 |
रासायनिक अभिक्रिया में पदार्थ न तो बनाया जा सकता है और न ही नष्ट किया जा सकता है। इस द्रव्यमान संरक्षण के नियम को सन्तुष्ट करने के लिए रासायनिक समीकरणों को सन्तुलित किया जाता है।
प्रश्न 5.
निम्नलिखित कथनों को रासायनिक समीकरण के रूप में परिवर्तित कर उन्हें सन्तुलित कीजिए –
(a) नाइट्रोजन गैस हाइड्रोजन गैस से संयोग करके अमोनिया बनाती है।
(b) हाइड्रोजन सल्फाइड गैस का वायु में दहन होने पर जल एवं सल्फर डाइऑक्साइड बनता है।
(c) ऐल्युमिनियम सल्फेट के साथ अभिक्रिया कर बेरियम क्लोराइड, ऐलुमिनियम क्लोराइड एवं बेरियम सल्फेट का अवक्षेप देता है।
(d) पोटैशियम धातु जल के साथ अभिक्रिया करके पोटैशियम हाइड्रॉक्साइड एवं हाइड्रोजन गैस देती
उत्तर-
(a) प्रश्नानुसार, नाइट्रोजन + हाइड्रोजन → अमोनिया
चरण 1.
सर्वप्रथम इसका प्रतीकात्मक समीकरण लिखकर उसके चारों ओर बॉक्स खींचते हैं
H2 (g) + N2 (g) → NH3 (g)
चरण 2.
इस असन्तुलित समीकरण में उपस्थित विभिन्न तत्त्वों के परमाणुओं की संख्या की सूची बनाते हैं –
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| N | 2 | 1 |
| H | 2 | 3 |
चरण 3.
इस चरण में हाइड्रोजन के परमाणुओं की संख्या अधिक होने के कारण इनका सर्वप्रथम सन्तुलन करते
| हाइड्रोजन परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 2 (H2 में) | 3 (NH3 में) |
| सन्तुलन हेतु | 2×3 | 3×2 |
अ तः दिया गया समीकरण सन्तुलित होकर निम्नवत् होगा
3H2(g) + N2(g) → 2NH3 (g)
![]()
चरण 4.
चरण 3 में प्राप्त समीकरण में हाइड्रोजन व नाइट्रोजन के परमाणुओं की संख्या दोनों ओर समान है, अतः दिया गया समीकरण पूर्ण रूप से सन्तुलित है।
3H2(g) + N2(g) → 2NH3(g)
(b) कथन के अनुसार रासायनिक समीकरण निम्नवत् है –
H2S (g) + O2 (g) → SO2(g) + H2O (l)
इसे सन्तुलित करने के लिए निम्नलिखित चरणों को अपनाते हैं-
चरण 1. सर्वप्रथम प्रत्येक सूत्र के चारों ओर बॉक्स बनाते हैं –
H2S (g) + O2 (g) → SO2 (g) + H2O (l)
चरण 2. इस समीकरण में उपस्थित विभिन्न तत्वों के परमाणुओं की सूची बनाते हैं-
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| H | 2 | 2 |
| S | 1 | 1 |
| O | 2 | 3 |
चरण 3.
सर्वप्रथम हम ऑक्सीजन के परमाणुओं का सन्तुलन करते हैं –
| ऑक्सीजन के परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 2 (O2 में) | 3 (SO2 तथा H2O में) |
| सन्तुलन के लिए | 2×3 | 3×2 |
अत: इस गणना के उपरान्त समीकरण निम्नवत् होगा –
H2S (g) + 3O2 (g) → 2SO2 (g) +2H2O (l)
चरण 4.
चरण 3 में ऑक्सीजन परमाणुओं को सन्तुलित करने के कारण हाइड्रोजन के परमाणु असन्तुलित हो जाते हैं। अतः अब हाइड्रोजन के परमाणुओं को सन्तुलित करते हैं –
| हाइड्रोजन के परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 2 (H2S में) | 4(H2O में) |
| सन्तुलन के लिए | 2×2 | 4 |
पुनः आंशिक रूप से सन्तुलित समीकरण निम्नवत् त् होगा-.
2H2S (g) + 3O2 (g) →2SO2 (g) + 2H2O (l)
चरण 5. अब सल्फर के परमाणुओं की संख्या देखने पर ज्ञात होता है कि सल्फर के परमाणुओं की संख्या बाएँ व दाएँ पक्षों में बराबर है।
चरण 6. अतः अन्त में उपर्युक्त सन्तुलित समीकरण को – लिख देते हैं
2H2S (g) +3O2 (g) →2SO2 (g) + 2H2O(l)
(c) कथन के अनुसार असन्तुलित रासायनिक समीकरण निम्नवत् है –
BaCl2 (aq) +Al2(SO4)3 (aq) →AICl3 (aq) +BaSO4↑
इस समीकरण के सन्तुलन के लिए निम्नलिखित चरण अपनाए जाते हैं-
चरण 1.
सर्वप्रथम अभिक्रिया में प्रत्येक सूत्र को बॉक्स में लिख लेते हैं
BaCl2 (aq) + Al2 (SO4)3 (aq) →
AlCl3 (aq) + BaSO4]
चरण 2. विभिन्न तत्वों के परमाणुओं की संख्या के लिए सारणी –
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| Ba | 1 | 1 |
| Cl | 2 | 3 |
| Al | 2 | 1 |
| S | 3 | 1 |
| O | 12 | 4 |
चरण 3.
इस चरण में हम ऑक्सीजन परमाणुओं को सन्तुलित करेंगे –
| ऑक्सीजन के परमाणु । | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 12 [AI2(SO4)3, में] | 4 (BaSO4, में) |
| सन्तुलन के लिए | 12 | 3×4 |
उपर्युक्त गणना के उपरान्त आंशिक सन्तुलित समीकरण इस प्रकार होगा-
BaCl2 (aq) + Al2(SO4)3 (aq) → AlCl3 (aq) + 3BaSO4
चरण 4.
अब बेरियम के परमाणुओं की संख्या को सन्तुलन में लाते हैं –
| बेरियम के परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 1(BaCl2 में) | 3(BaSO4, में) |
| सन्तुलन के लिए | 3 ×1 | 3 |
पुनः आंशिक सन्तुलित समीकरण निम्नवत् होगा
3BaCl2 (aq) + Al2 (SO4)3 (aq) → AlCl3 (aq) + 3BaSO4 ↓
![]()
चरण 5.
इस चरण में हम क्लोरीन परमाणुओं की संख्या को सन्तुलित करेंगे –
| क्लोरीन के परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 6 (3 BaCl2, में) | 3(AlCl3, में) |
| सन्तुलन के लिए | 6 | 3×2 |
पुनः आंशिक सन्तुलित समीकरण निम्नवत् होगा –
3BaCl2 (aq) + Al2 (SO4)3 (aq) → 2AlCl3 (aq) + 3BaSO4 ↓
चरण 6.
दोनों पक्षों में सल्फर व ऐल्युमिनियम की संख्या समान है। अन्ततः दोनों पक्षों में सभी परमाणुओं की संख्या गिनकर हमें ज्ञात होता है कि यह समीकरण पूर्ण रूप से सन्तुलित है। इसे निम्न प्रकार लिखा जा सकता है –
3BaCl2 (aq) + Al2(SO4)3 (aq) → 2AlCl3 (aq) +3BaSO4 ↓
(d) कथन के अनुसार रासायनिक समीकरण इस प्रकार है-
K(s) + H2O(l) →KOH(aq) + H2↑ (g)
इस समीकरण के सन्तुलन के लिये निम्नलिखित चरण अपनाये जाते हैं-
चरण 1. सर्वप्रथम अभिक्रिया में प्रत्येक सूत्र को बॉक्स में लिख लेते हैं
K(s) + H2O(l) → KOH(aq) + H2↑(g)
चरण 2.
विभिन्न तत्वों के परमाणुओं की संख्या के लिये सारणी
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| K | 1 | 1 |
| H | 2 | 3 |
| O | 1 | 1 |
चरण 3.
इस चरण में हम हाइड्रोजन परमाणुओं को सन्तुलित करेंगे –
| हाइड्रोजन के परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 2(H2O) | 3 (KOH) तथा H2 |
| सन्तुलन के लिये | 2×3 | 3×2 |
अतः इस गणना के उपरान्त समीकरण निम्नवत् होगा –
K(s) + 3H2O → 2KOH(aq) + 2H2(g)
चरण 4.
चरण 3 में हाइड्रोजन परमाणु को सन्तुलित करने के कारण ऑक्सीजन परमाणु असन्तुलित हो जाते हैं। अतः अब ऑक्सीजन परमाणु को सन्तुलित करते हैं –
| ऑक्सीजन के परमाणु | अभिकारकों में | उत्पादों में |
| प्रारम्भ में | 3(H2O) | 2(KOH) |
| सन्तुलन के लिये | 3×2 | 2×3 |
अतः इस गणना के उपरान्त आंशिक सन्तुलित समीकरण इस प्रकार होगा-.
K(s) + 6H2O(l) → 6KOH(aq) + 3H2(g)
चरण 5.
अब K को सन्तुलित करने पर –
6K(s) + 6HH2O(l)→ 6KOH(aq) + 3HH2(g) ↑
चरण 6.
समीकरण को सरल बनाने के लिये अभिकारक व उत्पाद में 3 से भाग देने पर
2K(s) + 2H2O(l) → 2KOH(aq) + H2(g)↑.
उपरोक्त अभिक्रिया पूर्णतः सन्तुलित है।
प्रश्न 6.
निम्नलिखित रासायनिक समीकरणों को सन्तुलित कीजिए
(a) HNO3 +Ca(OH)2 →Ca(NO3)2 +H2O
(b) NaOH + H2SO4 →Na2SO4 +H2O
(c) NaCl+AgNO3 →AgCl+NaNO3
(d) BaCl + H2SO4 → BaSO4 + HCl
उत्तर-
(a)
चरण 1.
सर्वप्रथम प्रत्येक सूत्र के चारों ओर बॉक्स बनाते हैं –
HNO3 + Ca(OH)2 → Ca(NO3)2] + H2O
चरण 2.
समीकरण के तत्वों के परमाणुओं की सूची बनाते हैं –
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| H | 3 | 2 |
| N | 1 | 2 |
| O | 5 | 7 |
| Ca | 1 | 1 |
चरण 3. नाइट्रोजन तत्व के परमाणुओं को सन्तुलित करने के लिये HNO3 के पूर्व 2 लिखने पर
2HNO3 + Ca(OH)2 →Ca(NO3)2 + H2O
चरण 4. हाइड्रोजन के परमाणुओं को सन्तुलित करने के लिये HO अणुओं का गुणाः 2 से करने पर
2HNO3 + Ca(OH)2 →Ca(NO3)2 + 2H2O.
![]()
चरण 5.
चूँकि अभिकारक एवं उत्पादों में ऑक्सीजन परमाणुओं की संख्या समान अर्थात् 8 है, अतः अभिक्रिया अब पूर्ण रूप से सन्तुलित है।
2HNO3 + Ca(OH)2 →Ca(NO3)2 + 2H2O
(b) सर्वप्रथम अभिक्रिया में प्रत्येक सूत्र को बॉक्स में लिख लेते हैं
NaOH+ H2SO4→Na2SO4 + H2O
चरण 1.
विभिन्न तत्वों के परमाणुओं की संख्या के लिये सारणी –
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| Na | 1 | 2 |
| O | 5 | 5 |
| H | 3 | 2 |
| S | 1 | 1 |
चरण 2.
उपरोक्त प्रेक्षण से ज्ञात हो रहा है कि अभिक्रिया में ऑक्सीजन तथा सल्फर परमाणुओं की संख्या अभिकारक , व उत्पाद में समान है।
अत: Na के परमाणुओं की संख्या समान करने के लिये NaOH में 2 का गुणा करने पर-
2NaOH + H2SO4 → Na2SO4+ H2O
चरण 3.
हाइड्रोजन परमाणुओं की संख्या को समान करने के लिये H,0 में 2 का गुणा करने पर
2NaOH + H2SO4 →Na2SO4+ 2H2O
चरण 4.
अब अं सीजन परमाणुओं की संख्या दोनों तरफ देखने पर ज्ञात होता है कि यह दाँयी तरफ व बाँयी तरफ समान है। अतः यह अभिक्रिया एक सन्तुलित अभिक्रिया है।
2NaOH + H2 → Na2SO4+ 2H2O
(c) कथन के अनुसार असन्तुलित रासायनिक समीकरण निम्न है
NaCl + AgNO3 →AgCl + NaNO3
यह समीकरण पहले से ही सन्तुलित है, इसे सन्तुलित करने की कोई आवश्यकता नहीं है।
(d) कथन के अनुसार असन्तुलित रासायनिक समीकरण निम्न है –
BaCl2 (aq) + H2SO4 (aq) → BaSO4 (aq) + HCl(aq)
चरण 1.
सर्वप्रथम अभिक्रिया में प्रत्येक सूत्र को बॉक्स में लिख लेते हैं –
BaCl2 (aq) + H2SO4 (aq) → BaSO4 (aq) + HCl(aq)
चरण 2.
विभिन्न तत्वों के परमाणुओं की संख्या के लिये सारणी-
| तत्व | अभिकारकों में परमाणुओं की संख्या | उत्पादों में परमाणुओं की संख्या |
| Ba | 1 | 1 |
| Cl | 2 | 1 |
| H | 2 | 1 |
| S | 1 | 1 |
| O | 4 | 4 |
देखने पर विदित होता है कि अभिकारकों व उत्पादों में Ba, S व O की संख्या समान है।
चरण 3.
Cl– परमाणुओं की संख्या समान करने के लिये HCI में 2 का गुणा करने पर
BaCl2 + H2SO4 →BaSO4 + 2HCl
चरण 4.
देखने पर ज्ञात होता है कि अभिकारकों व उत्पादों में परमाणुओं की संख्या समान है अतः यह अभिक्रिया सन्तुलित है।
BaCl2 + H2SO4→BaSO4 + 2HCl
प्रश्न 7.
निम्न अभिक्रियाओं के लिए सन्तुलित रासायनिक समीकरण लिखिए –
(a) कैल्सियम हाइड्रॉक्साइड + कार्बन डाइऑक्साइड → कैल्सियम कार्बोनेट + जल
(b) जिंक + सिल्वर नाइट्रेट→ जिंक नाइट्रेट + सिल्वर
(c) ऐलुमिनियम + कॉपर क्लोराइड → ऐलुमिनियम क्लोराइड + कॉपर
(d) बेरियम क्लोराइड + पोटैशियम सल्फेट → बेरियम सल्फेट + पोटैशियम क्लोराइड
उत्तर –
(a) Ca(OH)2+CO2 →CaCO3 + H2O
(b) Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
(c) 2Al+3 CuCl2 → 2AlCl3 +3Cu
(d) BaCl +K2SO4 → BaSO4+2KCl
प्रश्न 8.
निम्न अभिक्रियाओं के लिए सन्तुलित रासायनिक समीकरण लिखिए एवं प्रत्येक अभिक्रिया का प्रकार बताइए-
(a) पोटैशियम ब्रोमाइड (aq) + बेरियम आयोडाइड (aq) → पोटैशियम आयोडाइड (aq) + बेरियम ब्रोमाइड (s)
(b) जिंक कार्बोनेट (s) → जिंक ऑक्साइड (s) + कार्बन डाइऑक्साइड (g)
(c) हाइड्रोजन (g) + क्लोरीन (g) → हाइड्रोजन क्लोराइड (g)
(d) मैग्नीशियम (s) + हाइड्रोक्लोरिक अम्ल (aq) → मैग्नीशियम क्लोराइड (aq) + हाइड्रोजन (g)
उत्तर –
(a) 2KBr(aq) +BaI2 (aq) →2KI (aq) +BaBr2 (s) (द्विविस्थापन अभिक्रिया)
(b) ZnCO3 (s)→ZnO (s) + CO2 (g) (वियोजन अभिक्रिया)
(c) H2(g) + Cl2 (g) → 2HCl(g) (संयोजन अभिक्रिया)
(d) Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2(g) (विस्थापन अभिक्रिया)
प्रश्न 9.
ऊष्माक्षेपी तथा ऊष्माशोषी अभिक्रियाओं का क्या अर्थ है ? उदाहरण दीजिए।
उत्तर-
ऊष्माक्षेपी अभिक्रिया-वे अभिक्रियाएँ जिनमें ऊष्मा उत्पन्न होती है, ऊष्माक्षेपी अभिक्रियाएँ कहलाती हैं। उदाहरण के लिए-मेथेन गैस वायु की ऑक्सीजन में जलकर कार्बन डाइऑक्साइड और जल वाष्प बनाती है। इसमें ऊष्मा भी उत्पन्न होती है।
CH4(g) + 2O2(g) → CO2(g)+22O (g) +ऊष्मीय ऊर्जा
ऊष्माशोषी अभिक्रिया-वे अभिक्रियाएँ जिनमें ऊष्मा का अवशोषण होता है, ऊष्माशोषी अभिक्रियाएँ कहलाती हैं।
उदाहरण के लिए-हाइड्रोजन तथा आयोडीन के संयोग से हाइड्रोजन आयोडाइड का बनना ऊष्माशोषी अभिक्रिया है।
H2 +I2 → 2 HI – ऊष्मा
![]()
प्रश्न 10.
श्वसन को ऊष्माक्षेपी अभिक्रिया क्यों कहते हैं ? वर्णन कीजिए।
उत्तर-
श्वसन की प्रक्रिया में ऊर्जा निर्मुक्त होती है। श्वसन के दौरान, हमारे शरीर की कोशिकाओं में ग्लूकोज (भोजन के पाचन से प्राप्त) वायु की ऑक्सीजन से संयुक्त होकर कार्बन डाइऑक्साइड तथा जल बनाने के साथ-साथ ऊर्जा को उत्सर्जित करता है।
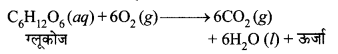
प्रश्न 11.
वियोजन अभिक्रिया को संयोजन अभिक्रियाओं के विपरीत क्यों कहा जाता है? इन अभिक्रियाओं के लिए समीकरण लिखिए।
उत्तर-
संयोजन अभिक्रिया में दो या दो से अधिक पदार्थ परस्पर संयोग करके एक नया पदार्थ बनाते हैं, जैसे
C(s)+O2 (g) → CO2(g)
तथा वियोजन अभिक्रिया में एक ही यौगिक विखण्डित होकर दो या दो से अधिक सरल पदार्थ बनाता है, जैसे कैल्सियम कार्बोनेट को गर्म करने पर वह वियोजित होकर कैल्सियम ऑक्साइड तथा कार्बन डाइऑक्साइड बनाता है।
![]()
इस प्रकार वियोजन अभिक्रिया, संयोजन अभिक्रिया के विपरीत है।
प्रश्न 12.
उन वियोजन अभिक्रियाओं के एक-एक समीकरण लिखिए जिनमें ऊष्मा, प्रकाश एवं विद्युत के रूप में ऊर्जा प्रदान की जाती है।
उत्तर-
(i) ऊष्मा के रूप में-कैल्सियम कार्बोनेट को गर्म करने पर यह अपघटित होकर कैल्सियम ऑक्साइड व कार्बन डाइऑक्साइड देता है।
![]()
(ii) प्रकाश के रूप में सूर्य के प्रकाश की उपस्थिति में सिल्वर क्लोराइड का सिल्वर तथा क्लोरीन में वियोजन हो जाता है।

(iii) विद्युत के रूप में-जब अम्लीकृत जल का वैद्युत अपघटन किया जाता है, वह अपघटित होकर हाइड्रोजन और ऑक्सीजन बनाता है।
![]()
प्रश्न 13.
विस्थापन एवं द्विविस्थापन अभिक्रियाओं में क्या अन्तर है ? इन अभिक्रियाओं के समीकरण लिखिए।
उत्तर-
(i) विस्थापन अभिक्रिया-ऐसी अभिक्रिया जिसमें किसी यौगिक के अणु के किसी एक परमाणु अथवा समूह (मूलक) के स्थान पर कोई दूसरा परमाणु अथवा समूह (मूलक) आ जाता है।
उदाहरण –

(ii) द्विविस्थापन अभिक्रिया-वह अभिक्रिया जिसमें आयनों का परस्पर विस्थापन होता है, द्विविस्थापन अभिक्रिया कहलाती है।
उदाहरण –

प्रश्न 14.
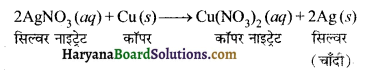
सिल्वर के शोधन में, सिल्वर नाइट्रेट के विलयन से सिल्वर प्राप्त करने के लिए कॉपर धातु द्वारा विस्थापन किया जाता है। इस प्रक्रिया के लिए अभिक्रिया लिखिए।
उत्तर –
प्रश्न 15.
अवक्षेपण अभिक्रिया से आप क्या समझते हैं ? उदाहरण देकर समझाइए।
उत्तर-
अवक्षेपण अभिक्रिया-ऐसी अभिक्रियाएँ जिनमें उत्पाद अविलेय अवस्था में प्राप्त होकर विलयन में नीचे स्थिर हो जाता है, अवक्षेप कहलाता है, तथा यह क्रिया अवक्षेपण अभिक्रिया कहलाती है।
उदाहरण –
Na2SO4 (aq) + BaCl2 (aq) → BaSO4(↓) +2NaCl (aq)
प्रश्न 16.
ऑक्सीजन के योग या ह्रास के आधार पर निम्न पदों की व्याख्या कीजिए। प्रत्येक के लिए दो उदाहरण दीजिए
(a) उपचयन
(b) अपचयन।
उत्तर-
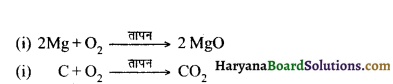
(a) उपचयन-वे अभिक्रियाएँ जिनमें ऑक्सीजन की वृद्धि (योग) होती है, उपचयन अभिक्रियाएँ कहलाती
उदाहरण –
(b) अपचयन।

प्रश्न 17.
एक भूरे रंग के चमकदार तत्व ‘X’ को वायु की उपस्थिति में गर्म करने पर वह काले रंग का हो जाता है। इस तत्व ‘X’ एवं उस काले रंग के यौगिक का नाम बताइए।
उत्तर-
तत्व ‘X’ कॉपर (Cu) है। काले रंग का यौगिक कॉपर (II) ऑक्साइड (CuO) है।
![]()
प्रश्न 18.
लोहे की वस्तुओं को हम पेण्ट क्यों करते
उत्तर-
लोहे की वस्तुओं पर जंग उनकी खुली सतह पर ऑक्सीजन एवं नमी के कारण लगती है। लोहे की वस्तुओं की सतह पर पेण्ट लगने से सतह खुली नहीं रहती तथा ऑक्सीजन वस्तु की सतह के सम्पर्क में नहीं आ पाती और वस्तु पर जंग नहीं लगती।
प्रश्न 19.
तेल एवं वसायुक्त खाद्य पदार्थों को नाइट्रोजन से प्रभावित क्यों किया जाता है ?
उत्तर-
तेल एवं वसायुक्त भोज्य पदार्थों के उपचयन से बचाव हेतु हम इनमें नाइट्रोजन प्रवाहित कर देते हैं। तेल तथा वसा का उपचयन होने पर ये विकृतगन्धी हो जाते हैं तथा इनकी गन्ध एवं स्वाद परिवर्तित हो जाता है। नाइट्रोजन प्रवाहित करने से इस प्रक्रिया को रोका जा सकता है।
प्रश्न 20.
निम्न पदों का वर्णन कीजिए तथा प्रत्येक का एक-एक उदाहरण दीजिए –
(a) संक्षारण,
(b) विकृतगन्धिता।
उत्तर-
(a) संक्षारण-जब किसी धातु की सतह वायु, जल अथवा अपने चारों ओर उपस्थित किसी अन्य पदार्थ द्वारा अभिक्रमित हो जाती है, अथवा इस पर जंग लग जाती है तब इसे संक्षारित वस्तु कहते हैं। यह प्रभाव संक्षारण कहलाता है। उदाहरण के लिए, लोहे पर जंग का लगना।
(b) विकृतगन्धिता-तेल व वसा के उपचयित हो जाने पर ये विकृतगन्धी हो जाते हैं तथा इनकी गन्ध व स्वाद में परिवर्तन हो जाता है। इनमें प्रतिऑक्सीकारक मिलाकर अथवा भोज्य पदार्थों को निर्वातित पात्रों में रखकर अथवा इनमें नाइट्रोजन प्रवाहित करके इस प्रक्रिया को रोका जा सकता है। उदाहरण-आलू की चिप्स की थैलियों में नाइट्रोजन प्रवाहित करके इन्हें उपचयित होने से बचाया जा सकता है।
HBSE 10th Class Science रासायनिक अभिक्रियाएँ एवं समीकरण InText Questions and Answers
(पाठ्य-पुस्तक पृ. सं. 6)
प्रश्न 1.
वायु में जलाने से पहले मैग्नीशियम रिबन को साफ क्यों किया जाता है ?
उत्तर-
मैग्नीशियम वायु में उपस्थित ऑक्सीजन से संयोग करके मैग्नीशियम ऑक्साइड बना लेता है। मैग्नीशियम ऑक्साइड व अन्य अशुद्धियों-धूल कण व नमी आदि को हटाकर शुद्ध मैग्नीशियम प्राप्त करने के लिए इसे वायु में जलाने से पहले साफ करना आवश्यक है।
![]()
प्रश्न 2.
निम्नलिखित रासायनिक अभिक्रियाओं के लिए सन्तुलित समीकरण लिखिए
(i) हाइड्रोजन + क्लोरीन → हाइड्रोजन क्लोराइड
(ii) बेरियम क्लोराइड + ऐलुमिनियम सल्फेट बेरियम सल्फेट + ऐलुमिनियम क्लोराइड
(iii) सोडियम + जल → सोडियम हाइड्रॉक्साइड + हाइड्रोजन
उत्तर-
(i) H2+ Cl2 → 2HCl
(ii) 3BaCl2+Al2 (SO4)3 → 3BaSO4 +2AlCl 3
(iii) 2Na + 2H2O → 2NaOH + H2 ↓
प्रश्न 3.
निम्नलिखित अभिक्रियाओं के लिए उनकी अवस्था के संकेतों के साथ सन्तुलित रासायनिक समीकरण लिखिए-
(i) जल में बेरियम क्लोराइड तथा सोडियम सल्फेट के विलयन अभिक्रिया करके सोडियम क्लोराइड का विलयन तथा अघुलनशील बेरियम सल्फेट का अवक्षेप बनाते हैं।
(ii) सोडियम हाइड्रॉक्साइड का विलयन (जल में) हाइड्रोक्लोरिक अम्ल के विलयन (जल में) से अभिक्रिया करके सोडियम क्लोराइड का विलयन तथा जल बनाते
उत्तर-

(पाठ्य-पुस्तक पृ. सं. 11)
प्रश्न 1.
किसी पदार्थ ‘X’ के विलयन का उपयोग सफेदी करने के लिए होता है।
(i) पदार्थ ‘X’ का नाम तथा इसका सूत्र लिखिए।
(ii) ऊपर (i) में लिखे पदार्थ ‘X’ की जल के साथ अभिक्रिया लिखिए।
उत्तर-
(i) पदार्थ ‘X’ का नाम कैल्सियम ऑक्साइड (शुष्क चूना) है, तथा इसका रासायनिक सूत्र Cao है।
(ii) CaO की जल के साथ अभिक्रिया निम्नलिखित

प्रश्न 2.
क्रियाकलाप 1.7 में एक परखनली में एकत्रित गैस की मात्रा दूसरी से दोगुनी क्यों है? उस गैस का नाम बताइए।
उत्तर-
क्रियाकलाप 1.7 में जल के विद्युत्-अपघटन की अभिक्रिया निम्नलिखित प्रकार होती है
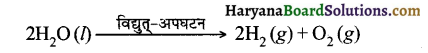
इस अभिक्रिया में हाइड्रोजन तथा ऑक्सीजन गैस 2 : 1 की मात्रा में प्राप्त होती है। द्रव्यमान संरक्षण के नियमानुसार जब जल के दो अणु अपघटित होते हैं तब उत्पन्न हुई हाइड्रोजन की मात्रा ऑक्सीजन की मात्रा से दोगुनी होती है। अतः एक परखनली में हाइड्रोजन गैस की मात्रा दोगुनी है।
(पाठ्य-पुस्तक पृ. सं. 15)
प्रश्न 1.
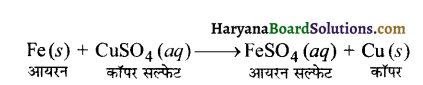
जब लोहे की कील को कॉपर सल्फेट के विलयन में डुबोया जाता है तो विलयन का रंग क्यों बदल जाता है ?
उत्तर-
जब लोहे की कील को कॉपर सल्फेट के विलयन में डुबोया जाता है तो लोहे की कील कॉपर सल्फेट के विलयन में से कॉपर को विस्थापित कर देती है तथा आयरन सल्फेट बनता है। अतः आयरन सल्फेट के विलयन के बनने के कारण विलयन का रंग बदल जाता है तथा लोहे की कील पर भूरे रंग की परत जम जाती है, एवं विलयन का रंग हल्का हरा हो जाता है।
प्रश्न 2.
क्रियाकलाप 1.10 से भिन्न द्विविस्थापन अभिक्रिया का एक उदाहरण दीजिए।
उत्तर-

प्रश्न 3.
निम्न अभिक्रियाओं में उपचयित तथा अपचयित पदार्थों की पहचान कीजिये
(i) 4Na (s) + O2 (g) →2Na2O(s)
(ii) CuO (s) + H2 (g) → Cu(s) + H2 O(l) [राज. 2015]
उत्तर-
(i) 4Na (s) + O2 (g) →2Na2O(s)
इस अभिक्रिया में सोडियम (Na) सोडियम ऑक्साइड (Na2O) में उपचयित या ऑक्सीकृत हो रहा है। इसका अर्थ यह है कि ऑक्सीजन का अपचयन हो रहा है।
(ii) CuO (s) + H2 (g) →Cu (s) + H2O(l)
इस अभिक्रिया में हाइड्रोजन गैस (H2) जल (H2O) में ऑक्सीकृत या उपचयित हो रही है जबकि कॉपर (ii) ऑक्साइड (CuO) का अपचयन कॉपर में हो रहा है|
HBSE 10th Class Science रासायनिक अभिक्रियाएँ एवं समीकरण InText Activity Questions and Answers
क्रियाकलाप 1.1. (पा. पु. पृ. सं. 1)
प्रश्न 1.
आपने क्या प्रेक्षण किया?
उत्तर-
हमने देखा कि मैग्नीशियम रिबन चमकदार श्वेत लौ के साथ जलकर श्वेत चूर्ण में परिवर्तित हो जाता है।
प्रश्न 2.
यह श्वेत चूर्ण किस यौगिक का है?
उत्तर-
यह श्वेत चूर्ण मैग्नीशियम ऑक्साइड का है। यह वायु में उपस्थित ऑक्सीजन तथा मैग्नीशियम के बीच होने वाली अभिक्रिया के कारण बनता है।
क्रियाकलाप 1.2 (पा. पु. पृ. सं. 2)
प्रश्न 1.
आपको कैसे ज्ञात हुआ कि रासायनिक परिवर्तन हुआ है?
उत्तर-
क्योंकि अभिक्रिया के दौरान अभिकारकों की अवस्था व रंग परिवर्तित हुआ है।
प्रश्न 2.
इस क्रियाकलाप का रासायनिक समीकरण लिखें।
उत्तर-

क्रियाकलाप 1.3 (पा. पु. पृ. सं. 2)
प्रश्न 1.
क्या जस्ते के दानों के आसपास कुछ होता दिखायी दे रहा है?
उत्तर-
हाँ, वहाँ से गैस के बुलबुले उत्पन्न होते दिखाई दे रहे हैं एवं जस्ते के दानों का आकार धीरे-धीरे घटता जा रहा है।
प्रश्न 2.
ये बुलबुले किस गैस के हैं?
उत्तर-
ये बुलबुले हाइड्रोजन गैस के हैं।
![]()
प्रश्न 3.
शंक्वाकार फ्लास्क या परखनली को स्पर्श कीजिए। क्या इसके तापमान में कोई परिवर्तन हो रहा है?
उत्तर-
शंक्वाकार फ्लास्क गर्म हो रहा है। इसका तापमान बढ़ रहा है।
प्रश्न 4.
क्रियाकलापका रासायनिक समीकरण लिखें।
उत्तर-
शब्द समीकरणजस्ता + सल्फ्यूरिक अम्ल → जिंक सल्फेट + हाइड्रोजन रासायनिक समीकरण
Zn(s) + H2SO4 (aq) → ZnSO4(aq) + H2(g)
क्रियाकलाप 1.4 (पा. पु. पृ. सं. 7)
प्रश्न 1.
क्या बीकर के ताप में कोई परिवर्तन हुआ?
उत्तर-
हाँ, बीकर अत्यन्त गर्म हो गया।
प्रश्न 2.
अभिक्रिया का समीकरण लिखें।
उत्तर-
कैल्सियम ऑक्साइड जल के साथ तीव्रता से । अभिक्रिया करके बुझे हुए चूने (कैल्सियम हाइड्रॉक्साइड) का निर्माण करके अधिक मात्रा में ऊष्मा उत्पन्न करता है।

क्रियाकलाप 1.5 (पा. पु. पृ. सं. 8) .
प्रश्न 1.
गर्म करने के पश्चात् क्रिस्टल के रंग में क्या है परिवर्तन होता है?
उत्तर-
गर्म करने से पहले क्रिस्टल का रंग हरा था जो कि गर्म करने के पश्चात् भूरा हो गया ।

प्रश्न 2.
यह किस प्रकार की वियोजन अभिक्रिया है?
उत्तर-
यह ऊष्मीय वियोजन अभिक्रिया है। ‘
क्रियाकलाप 1.7 (पा. पु. पृ. सं. 9)
प्रश्न 1.
लेड नाइट्रेट को गर्म करने पर क्या परिवर्तन हुआ?
उत्तर-
लेड नाइट्रेट को गर्म करने पर भूरे रंग का धुआँ उत्सर्जित होता है। यह भूरे रंग का धुआँ, नाइट्रोजन डाइऑक्साइड गैस में बनने के कारण होता है।

प्रश्न 2.
यह भूरे रंग का धुआँ किस पदार्थ का है?
उत्तर-
यह भूरे रंग का धुआँ नाइट्रोजन डाइऑक्साइड के (NO2) का है।
![]()
क्रियाकलाप 1. 8 (पा. पु. पृ. सं. 10)
प्रश्न 1.
एक जलती हुई मोमबत्ती को परखनलियों के मुख पर ले जाने से क्या होता है?
उत्तर-
- जिस परखनली में ऑक्सीजन गैस भरी है, उसके मुख पर जलती हुई मोमबत्ती को ले जाने पर यह तेजी से जलने लगती है।
- जिस परखनली में हाइड्रोजन गैस भरी है, उसके मुख पर जलती हुई मोमबत्ती ले जाने पर यह पॉप-आवाज (POP-SOUND) के साथ जलती है।
प्रश्न 2.
दोनों परखनलियों में कौन सी गैस उपस्थित है?
उत्तर-
एक परखनली में हाइड्रोजन गैस व दूसरी परखनली में ऑक्सीजन गैस भरी हुई है।
प्रश्न 3.
इस प्रकार के अपघटन को क्या कहते हैं?
उत्तर-
इस अपघटन को विद्युत-अपघटन कहते हैं|
प्रश्न 4.
क्या दोनों परखनलियों में एकत्रित गैस का आयतन समान है?
उत्तर-
नहीं, दोनों परखनलियों में एकत्रित गैस का आयतन समान नहीं है।
प्रश्न 5.
किस गैस का आयतन ज्यादा है?
उत्तर-
हाइड्रोजन गैस का आयतन ज्यादा है।
प्रश्न 6.
किस गैस का आयतन कम है?
उत्तर-
ऑक्सीजन गैस का आयतन कम है।
क्रियाकलाप 1.8 (पा. पु. पृ. सं. 10)
प्रश्न 1.
धूसर रंग किस धातु के कारण हो जाता है?
उत्तर-
धूसर रंग सिल्वर धातु के कारण हो जाता है।
प्रश्न 2.
थोड़ी देर पश्चात् सिल्वर क्लोराइड के रंग को देखिए क्या परिवर्तन हुआ?
उत्तर-
सूर्य के प्रकाश में श्वेत रंग का सिल्वर क्लोराइड धूसर रंग का हो जाता है। प्रकाश की उपस्थिति में सिल्वर क्लोराइड का सिल्वर तथा क्लोरीन में वियोजन के कारण से ऐसा होता है।
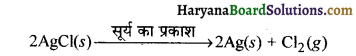
प्रश्न 3.
यदि सिल्वर ब्रोमाइड को भी कुछ समय के लिये प्रकाश में रखें तो क्या यह भी इसी प्रकार अभिक्रिया करेगा?
उत्तर-
हाँ, यदि सिल्वर ब्रोमाइड को कुछ समय के लिए प्रकाश में रखें तो यह भी धूसर रंग में परिवर्तित हो जाता है जो कि सिल्वर ब्रोमाइड के सिल्वर तथा ब्रोमाइड में वियोजन के कारण होता है।

प्रश्न 4.
सिल्वर ब्रोमाइड के वियोजन की यह अभिक्रिया कहाँ प्रयुक्त होती है?
उत्तर-
सिल्वर ब्रोमाइड के वियोजन की इस अभिक्रिया का प्रयोग श्वेत-श्याम फोटोग्राफी में किया जाता है।
![]()
प्रश्न 5.
किस प्रकार की ऊर्जा के कारण यह वियोजन अभिक्रिया होती है?
उत्तर-
प्रकाशीय ऊर्जा के कारण यह वियोजन अभिक्रिया होती है।
यह भी करके देखिये –
एक परखनली में लगभग 2 ग्राम बेरियम हाइड्रॉक्साइड लीजिए अब इसमें लगभग 1 ग्राम अमोनियम क्लोराइड डालकर काँच की छड़ से मिलाइये। अपनी हथेली से परखनली के निचले सिरे को स्पर्श कीजिये। आप क्या अनुभव करते हैं? यह कौन सी अभिक्रिया है?
उत्तर-
बेरियम हाइड्रॉक्साइड एवं अमोनियम क्लोराइड को मिलाने में निम्न अभिक्रिया होती है –
Ba (OH)2(s) + 2NH4Cl(aq) → BaCl2(aq) + 2NH4OH(aq) परखनली को छूने पर हमें ठंड का अनुभव होता है अर्थात् परखनली ठंडी हो जाती है। यह एक द्विविस्थापन एवं ऊष्माशोषी अभिक्रिया है।
क्रियाकलाप 1.9 (पा. पु. पृ. सं. 11)
प्रश्न 1.
परखनली (A) में रखे कॉपर सल्फेट विलयन का रंग क्या है?
उत्तर-
परखनली (A) में रखे कॉपर सल्फेट विलयन का रंग नीला हो जाता है।
प्रश्न 2.
परखनली (B) में रखे कॉपर सल्फेट विलयन का रंग क्या है?
उत्तर-
परखनली (B) में रखे कॉपर सल्फेट विलयन का नीला रंग बहुत हल्का हो जाता है।
प्रश्न 3.
लोहे की कील का रंग भूरा क्यों हो गया?
उत्तर-
लोहे की कील का रंग कॉपर के अवक्षेपण के कारण भूरा हो जाता है।
CuSO4 +Fe → FeSO4 +Cu
प्रश्न 4.
कॉपर सल्फेट के विलयन का नीला रंग मलीन क्यों पड़ गया?
उत्तर-
कॉपर सल्फेट के विलयन का नीला रंग आयरन सल्फेट के बन जाने के कारण मलीन हो गया।
![]()
प्रश्न 5.
यह अभिक्रिया किस प्रकार की अभिक्रिया
उत्तर-
यह अभिक्रिया विस्थापन अभिक्रिया है।
![]()
प्रश्न 6.
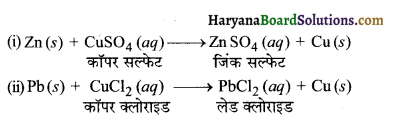
विस्थापन अभिक्रिया के कुछ अन्य उदाहरण क्या हैं?
उत्तर-
कुछ अन्य उदाहरण
क्रियाकलाप 1.10 (पा. पु. पृ. सं. 12)
प्रश्न 1.
सफेद अवक्षेप किस पदार्थ का है?
उत्तर-
सफेद अवक्षेप बेरियम सल्फेट (BaSO4) का है।
प्रश्न 2.
अभिक्रिया के लिये सन्तुलित रासायनिक समीकरण दीजिए।
उत्तर-
सन्तुलित रासायनिक समीकरण निम्न है –

प्रश्न 3.
क्या यह भी एक द्विविस्थापन अभिक्रिया
उत्तर-
हाँ, यह एक द्विविस्थापन अभिक्रिया है।
प्रश्न 4.
अभिक्रिया के दौरान बने सह-उत्पाद सोडियम क्लोराइड का क्या होता है?
उत्तर-
अभिक्रिया के दौरान बना सह-उत्पाद सोडियम क्लोराइड विलयन में ही रहता है।
प्रश्न 5.
द्विविस्थापन अभिक्रियाएँ किन्हें कहते हैं?
उत्तर-
वे अभिक्रियाएँ जिनमें अभिकारकों के आयनों का आदान-प्रदान होता है, द्विविस्थापन अभिक्रियाएँ कहलाती हैं।
क्रियाकलाप 1.11 (पा. पु. पृ. सं. 13)
प्रश्न 1.
कॉपर चूर्ण को गर्म करने पर आपने क्या देखा?
उत्तर-
कॉपर चूर्ण काला पड़ जाता है।
प्रश्न 2.
कॉपर चूर्ण काला क्यों पड़ जाता है?
उत्तर-
क्योंकि कॉपर चूर्ण की सतह पर कॉपर ऑक्साइड (II) की काली पर्त चढ़ जाती है।
